Praseodimio, Pr, número atómico 59
General
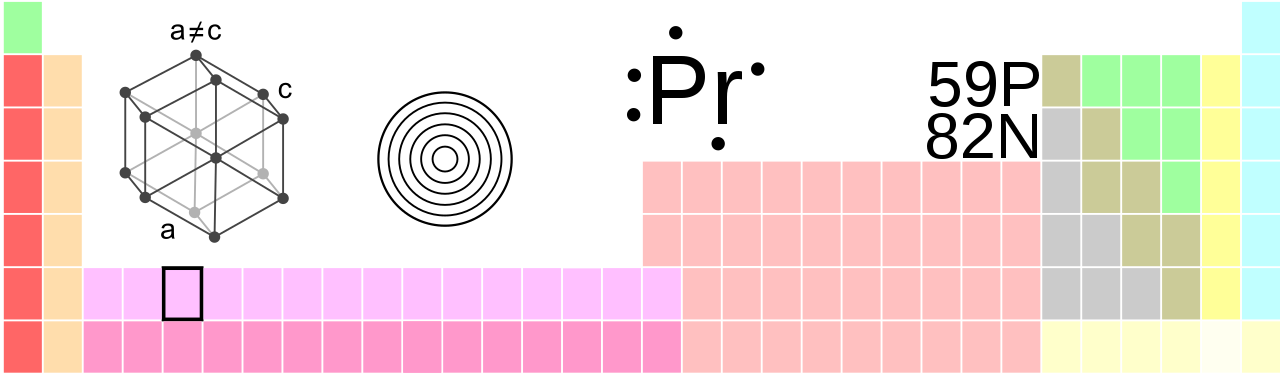
El praseodimio es un elemento químico con el símbolo del elemento Pr y el número atómico 59. En la tabla periódica pertenece al grupo de los lantánidos y, por lo tanto, también pertenece a los metales de las tierras raras. Del color verde de sus compuestos proviene el nombre: la palabra griega prásinos significa "puerro verde", didymos "doble" o "gemelo".
1841 Carl Gustav Mosander extrajo el Didym de tierras raras del óxido de lantano. 1874 comentó a Per Teodor Cleve que Didym era en realidad dos elementos. En el año 1879 Lecoq de Boisbaudran samario aislado de Didym, que ganó del mineral Samarskit. 1885 logró separar a Carl Auer von Welsbach, Didym en Praseodimio y Neodimio, que forman ambas sales de diferentes colores.
Praseodimio es un compañero en los minerales típicos de tierras raras Cerit, Monazit y Bastnäsit. Las reservas mundiales se estiman en 4 millones de toneladas.
recuperación
Como con todos los lantánidos, los minerales se enriquecen primero por flotación, luego los metales se convierten en haluros correspondientes y se separan por cristalización fraccionada, intercambio iónico o extracción. El metal se obtiene por electrólisis de sal fundida o reducción de calcio.
Características
El praseodimio es un metal paramagnético blanco plateado blando, que pertenece a los lantánidos y metales de tierras raras. Es un poco más resistente a la corrosión en el aire que el europio, el lantano o el cerio, pero forma fácilmente una capa de óxido verde que se desprende en el aire. A 798 ° C, el α-Pr hexagonal se convierte en el β-Pr cúbico centrado en el cuerpo. El praseodimio natural se compone únicamente del isótopo estable 141Pr. Se conocen otros 38 isótopos radiactivos, siendo 143Pr y 142Pr los más longevos, con vidas medias de 13,57 días y 19,12 horas, respectivamente. Todos los demás isótopos tienen vidas medias de menos de 5,985 horas, y la mayoría incluso menos de 33 segundos. También hay 6 estados metaestables, siendo 138mPr (t½ 2,12 horas), 142mPr (t½ 14,6 minutos) y 134mPr (t½ 11 minutos) los más estables.
Los isótopos tienen un rango de masa atómica de 120,955 (121Pr) a 158,955 (159Pr). Debido a su sensibilidad al aire, el praseodimio debe almacenarse bajo gasolina o sellarse en plástico o vidrio.
No se conoce un significado biológico, pero se dice que los compuestos de praseodimio son ligeramente dañinos para el hígado. Sin embargo, no hay valores de toxicidad.
El praseodimio ocurre en sus compuestos trivalentes y tetravalentes, siendo el número de oxidación trivalente el más abundante. Los iones Pr (III) son de color verde amarillo y los iones Pr (IV) son incoloros. Bajo condiciones reductoras particulares y praseodimio divalente se puede realizar, por. Por ejemplo, en Pr2I5.
Se conocen varios haluros de todas las etapas, por ejemplo PrF3, PrF4, PrCl3, PrBr3, PrI3, Pr2I5. Los haluros trivalentes forman diferentes hidratos.
También hay varios compuestos con calcógenos: el óxido de praseodimio (III, IV) marrón-negro normal Pr6O11, el PrO2 casi negro, el Pr2O3 verde, Pr2S3, Pr2Te3 y otros compuestos binarios como PrN, PrP. Además, el praseodimio está presente en varias sales, como el nitrato de praseodimio higroscópico Pr (NO3) 3.xH2O, el sulfato de praseodimio bellamente cristalizado Pr2 (SO4) 2.8 H2O y otros.
Además, forma varios complejos de fluorido tales. Por ejemplo, el K2 [PrF6] con Pr cuadrivalente.
Utilizar
El praseodimio se usa en aleaciones con magnesio para la producción de metal de alta resistencia para motores de aviones.
Las aleaciones de cobalto y hierro son fuertes imanes permanentes.
Los compuestos de praseodimio se utilizan para colorear el vidrio y el esmalte (por ejemplo, en lentes de faro de color verde en tecnología de iluminación).
Los compuestos también mejoran la absorción de rayos UV y se usan para gafas de protección ocular durante la soldadura.
| General | |
| Nombre, símbolo
ordinal |
Praseodimio, Pr, 59 |
| serie | lantánidos |
| Grupo, periodo, bloque | La, 6, f |
| Apariencia | blanco plateado, amarillento |
| CAS | 7440-10-0 |
| Fracción masiva de la envoltura de la tierra | 5,2 ppm |
| nuclear | |
| masa atómica | 140,90765 u |
| radio atómico | . |
| Radio covalente | . |
| Elektronenkonf. | [Xe] 4f (3) 6s2 |
| 1. ionización | 527,0 KJ / mol |
| 2. ionización | 1020 KJ / mol |
| 3. ionización | 2086 KJ / mol |
| físicamente | |
| estado físico | fest |
| estructura cristalina | hexagonal |
| densidad | 6,475 g / cm3 (25 ° C) |
| magnetismo | paramagnético (χm = 2,9 * 10 (-3)) |
| punto de fusión | 1208 K (935 C) |
| punto de ebullición | 3563 K (3290 C) |
| Volumen molar | 20,80 * 10 (-6) m (3) / mol |
| El calor de vaporización | 330 KJ / mol |
| calor de fusión | 6,9 KJ / mol |
| Conductividad electrica | 1,43 * 10 (6) A / (V * m) |
| conductividad térmica | 13 W / (m * K) |
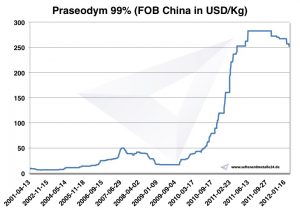
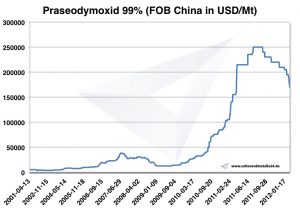
Precio del praseodimio
Precios de praseodimio -> precios de tierras raras