Samario, Sm, número atómico 62
General
El samario (después del mineral Samarskit, que a su vez lleva el nombre del ingeniero de minas WM Samarski) es un elemento químico con el símbolo del elemento Sm y el número atómico 62. En la tabla periódica, el elemento plateado brillante está en el grupo de los lantánidos y, por lo tanto, también pertenece a los metales de las tierras raras.
Para el descubrimiento del Samario, hay varias representaciones en la literatura.
1. 1853 mostró el samario suizo Jean Charles Galissard de Marignac espectroscópicamente por una línea de absorción afilada en el Didymoxid después. 1879 aisló al francés Paul Emile Lecoq de Boisbaudran el elemento del mineral Samarskit (Y, Ce, U, Fe) 3 (Nb, Ta, Ti) 5O16). La designación de minerales y elementos se deriva del inspector minero ruso Coronel Samarsky, quien descubrió el mineral.
2. 1878 descubrió al químico suizo Marc Delafontaine Samarium, al que llama Decipum, en óxido de didimio. 1879 descubre de forma independiente el Samario Paul Emile Lecoq de Boisbaudran. 1881 muestra a Delafontaine que su elemento aislado contiene otro elemento además del samario.
3. El descubrimiento espectroscópico 1 de Marignac de 1853, mencionado bajo 1878, fue realizado por XNUMX por Paul Emile Lecoq de Boisbaudran.
1903, el químico alemán Wilhelm Muthmann produjo samario metálico por electrólisis.
Por supuesto, el samario elemental no ocurre. Sin embargo, algunos minerales como la monazita, la bastnasita y la samarskita contienen el elemento. Monazita contiene hasta 1% de samario.
recuperación
A partir de la monazita o la bastnasita, se produce la separación de las tierras raras mediante intercambio iónico, extracción con solventes o deposición electroquímica. En una etapa final del proceso, el óxido de samario de alta pureza con lantano metálico se reduce al metal y se sublima.
Características
El samario es razonablemente estable en el aire, forma una capa de óxido amarillento pasivante. El samario metálico brillante se enciende por encima de 150 ° C. Reacciona con el oxígeno para formar sesquióxido Sm2O3. Reacciona violentamente con el agua para formar hidrógeno e hidróxido de samario. Como ocurre con todos los lantanoides, el estado de oxidación más estable es +3. Samario viene en tres modificaciones. Los puntos de transición son 734 ° C y 922 ° C. Los cationes Sm3 + vuelven amarillas las soluciones acuosas.
Hay cuatro isótopos radiactivos estables y 19 inestables. Los isótopos naturales más comunes son 152Sm (26,7%), 154Sm (22,7%) y 147Sm (15%).
Utilizar
Junto con otras tierras raras para lámparas de arco de carbono para sistemas de proyección de películas.
Dopaje de cristales individuales de fluoruro de calcio para maser y láser.
Debido a su gran sección transversal de neutrones térmicos y epitermales, el samario se utiliza como absorbente de neutrones en aplicaciones nucleares.
Imanes de samario cobalto:
Los imanes permanentes SmCo5 tienen una alta resistencia a la desmagnetización y una fuerza coercitiva de hasta 2200 kA / m. La aleación Sm2Co17 mejorada es más costosa de producir, pero tiene propiedades magnéticas más altas y mayor resistencia a la corrosión.
Se utilizan en motores paso a paso para relojes de cuarzo, motores de accionamiento en dispositivos de cinta en miniatura (walkman, dictáfonos), auriculares, sensores, acoplamientos en agitadores y unidades de disco duro. Como materiales magnéticos que ahorran peso, también se usan en aplicaciones aeroespaciales.
El óxido de samario se agrega al vidrio óptico para la absorción de la luz infrarroja.
Los compuestos de samario se usan para sensibilizar el fósforo (fósforo) cuando se irradian con luz infrarroja.
Como catalizador; El óxido de samario cataliza la hidrogenación y deshidrogenación de etanol (alcohol).
En medicina, el isótopo 153Samario se usa junto con un bisfosfonato (Lexidronam) para el tratamiento del dolor óseo en los cánceres (terapia con radionúclidos para metástasis óseas).
Los compuestos con samario en el estado de oxidación menos favorable + 2 (especialmente yoduro de samario (II) y bromuro de samario (II)) encuentran aplicación en la síntesis orgánica (agente reductor y reactivo de transferencia de un electrón, p. Ej., Acoplamientos de pinacol mediados por samario) ,
En combinación con el etilendiaminotetra (ácido metilenofosfónico) radiofarmacéutico en medicina nuclear para el tratamiento paliativo de metástasis óseas y esqueléticas.
| General | |
| Nombre, símbolo
ordinal |
Samario, Sm, 62 |
| serie | lantánidos |
| Grupo, periodo, bloque | La, 6, f |
| Apariencia | blanco plateado |
| CAS | 7440-19-9 |
| Fracción masiva de la envoltura de la tierra | 6 ppm |
| nuclear | |
| masa atómica | 150,36 u |
| radio atómico | . |
| Radio covalente | . |
| Elektronenkonf. | [Xe] 4f (6) 6s2 |
| 1. ionización | 544,5 KJ / mol |
| 2. ionización | 1070 KJ / mol |
| 3. ionización | 2260 KJ / mol |
| físicamente | |
| estado físico | fest |
| estructura cristalina | trigonal |
| densidad | 7,536 g / cm3 (25 ° C) |
| magnetismo | paramagnético (χm = 1,12 * 10 (-3)) |
| punto de fusión | 1345 K (1072 C) |
| punto de ebullición | 2076 K (1803 C) |
| Volumen molar | 19,98 * 10 (-6) m (3) / mol |
| El calor de vaporización | 175 KJ / mol |
| calor de fusión | 8,6 KJ / mol |
| Conductividad electrica | 1,06 * 10 (6) A / (V * m) |
| conductividad térmica | 13 W / (m * K) |
Precios del samario
Precios del samario -> precios de las tierras raras
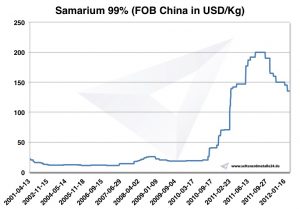
Gráfico Samario 2001-2012
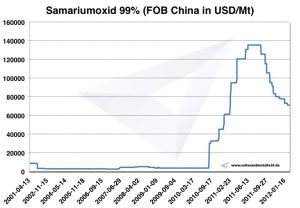
Gráfico de óxido de samario 2001-2012