Itrio, Y, número atómico 39
General
El itrio [ʏtriʊm] es un elemento químico con el símbolo del elemento Y y el número ordinal 39. Pertenece a los metales de transición y los metales de tierras raras, en la tabla periódica está en el 5. Período, así como el 3. Subgrupo (grupo 3) o grupo escandio. Ittrium lleva el nombre del primer sitio, la mina Ytterby cerca de Estocolmo, así como Ytterbium, Terbium y Erbium.
Johan Gadolin 1794 descubrió el itrio (de Ytterby, mina cerca de la capital sueca, Estocolmo) en Mineral Ytterbit. 1824 fabricó el itrio contaminado de Friedrich Wöhler reduciendo el cloruro de itrio con potasio. Solo 1842 sucedió a Carl Gustav Mosander separando el itrio de los elementos que lo acompañan, erbio y terbio.
El itrio no se encuentra en la naturaleza en el estado elemental. Los minerales que contienen itrio (Yttererden) siempre están asociados con otros metales de tierras raras. También puede estar contenido en minerales de uranio. Las arenas de Monazita con hasta 3% de itrio y la bastnasita con 0,2% de itrio son comercialmente degradables. Además, es el componente principal de xenotima (Y [PO4]).
Gran Monazitvorkommen, el comienzo de 19. Descubiertos y explotados en Brasil e India en el siglo XX, estos dos países se convirtieron en grandes productores de minerales de itrio. Solo la apertura de la mina Mountain Pass en California, que produjo grandes cantidades de bastnasita hasta los 1990, convirtió a EE. UU. En el principal productor de itrio, aunque la bastnasita extraída allí contiene solo una pequeña cantidad de itrio. Desde el cierre de esta mina, China es el mayor productor de tierras raras de 60%. Estos se obtienen en una mina cerca de Bayan Kuang, cuyo mineral contiene xenotima, y de minerales arcillosos que absorben iones, que se extraen principalmente en el sur de China.

Itrio metal
recuperación
La separación de las tierras raras entre sí es un paso laborioso en la producción de itrio. La cristalización fraccionada de soluciones salinas fue el método preferido al principio, que se utilizó desde el principio para la separación a escala de laboratorio de las tierras raras. Solo la introducción de la cromatografía iónica permitió separar las tierras raras a escala industrial.
El óxido de itrio concentrado se convierte en fluoruro. La posterior reducción a metal se produce con calcio en el horno de inducción al vacío.
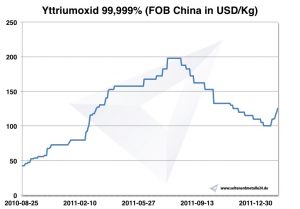
Gráfico de óxido de itrio 2010-2011
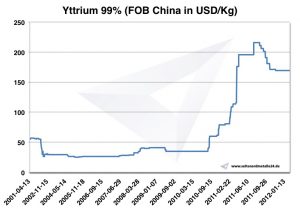
Gráfico de itrio 2001-2012
Características
El itrio es relativamente estable en el aire, pero se oscurece bajo la luz. A temperaturas superiores a 400 ° C, se pueden encender interfaces nuevas. El itrio finamente dividido es relativamente inestable. El itrio tiene una sección transversal de baja captura para neutrones.
Es principalmente trivalente en sus compuestos. Sin embargo, también hay compuestos agrupados en los que el itrio puede asumir estados de oxidación <3.
Hay un total de isótopos 32 entre 76Y y 108Y, así como otros isómeros centrales 24 conocidos. De estos, solo un 89Y, del cual existe exclusivamente el itrio natural, es estable. El itrio es uno de los elementos puros de 22. Los radioisótopos más estables son 88Y con una vida media de días 106,65 y 91Y con una vida media de días 58,51. Todos los demás isótopos tienen una vida media de menos de un día, con la excepción de 87Y, que tiene una vida media de 79,8 horas y 90Y con 64 horas. Los isótopos de itrio se encuentran entre los productos más comunes de fisión de uranio en reactores nucleares y en explosiones nucleares.
Tabla Periódica de itrio-39
Utilizar
El itrio metálico se utiliza en la tecnología de los reactores de tubos. Una aleación de itrio-cobalto se puede usar como un imán permanente. El itrio se utiliza como material para calentar cables en fuentes de iones de espectrómetros de masas. En la metalurgia, se utilizan aditivos menores de itrio para el refinado de granos, por ejemplo, en aleaciones conductoras de calor de hierro-cromo-aluminio, aleaciones de cromo, molibdeno, titanio y circonio. En aleaciones de aluminio y magnesio, tiene un efecto fortalecedor. Técnicamente más importantes son los compuestos de itrio oxídico:
Nitrato de itrio como material de recubrimiento en un manto
El granate de aluminio de itrio (YAG) sirve como cristal láser
Granate de hierro de itrio (YIG) como filtro de microondas
Zirconia estabilizada con itrio como electrolito sólido en celdas de combustible (SOFC, celda de combustible de óxido sólido)
Sin embargo, los usos más importantes de los óxidos de itrio y los sulfuros de óxido de itrio son la versatilidad en fósforos dopados (fósforos) de europio (rojo) y tulio (azul) trivalentes en tubos de imagen de televisión, lámparas fluorescentes y tubos de radar.
Además, las cerámicas y aleaciones de itrio se utilizan en:
sondas lambda
Superconductores (p. Ej. Óxido de itrio-bario-cobre YBa2Cu3O7-x)
aleaciones de SAO
chispa
Como un emisor beta puro, 90Yttrium se usa en medicina nuclear para la terapia, por ejemplo, Radiosynoviorthese.
El itrio se considera no esencial y tóxico (valor de MAK = 5 mg / m3).
| General | ||
| Nombre, símbolo
ordinal |
Itrio, Y, 39 | |
| serie | Los metales de transición | |
| Grupo, periodo, bloque | 3, 5, d | |
| Apariencia | blanco plateado | |
| CAS | 7440-65-5 | |
| Fracción masiva de la envoltura de la tierra | 26 ppm | |
| nuclear | ||
| masa atómica | 88,90585 u | |
| radio atómico | . | |
| Radio covalente | . | |
| Elektronenkonf. | [Kr] 4d (1) 5s2 | |
| 1. ionización | 600 KJ / mol | |
| 2. ionización | 1180 KJ / mol | |
| 3. ionización | 1980 KJ / mol | |
| físicamente | ||
| estado físico | fest | |
| estructura cristalina | hexagonal | |
| densidad | 4,472 g / cm3 | |
| magnetismo | paramagnético (χm = 1,2 * 10 (-4)) | |
| punto de fusión | 1799 K (1526 C) | |
| punto de ebullición | 3609 K (3336 C) | |
| Volumen molar | 19,88 * 10 (-6) m (3) / mol | |
| El calor de vaporización | 380 KJ / mol | |
| calor de fusión | 11,4 KJ / mol | |
| Conductividad electrica | 1,66 * 10 (6) A / (V * m) | |
| conductividad térmica | 17 W / (m * K) | |
