Germanio, Ge, número atómico 32
Precio de germanio, ocurrencia, extracción, uso
El germanio (del latín Germania 'Alemania', después del país en el que se encontró por primera vez) es un elemento químico con el símbolo del elemento Ge y el número atómico 32. En la tabla periódica está en el 4. Periodo y en el 4. Grupo principal (14, grupo IUPAC, bloque p y grupo de carbono). Estaba en 6. Febrero 1886 detectado por primera vez en argyrodita mineral.
Historia
Cuando Xnumx Dmitri Mendeleev diseñó la tabla periódica, descubrió una brecha debajo del silicio y postuló un elemento hasta ahora desconocido, al que llamó silicio Eka. Sin embargo, Mendeleev hizo predicciones sobre las propiedades del silicio Eka y sus compuestos, que fueron rechazados por la ciencia.
1885 descubrió que Clemens Winkler (1838-1904), químico de la Bergakademie Freiberg, cuando trabajaba con la argyrodita mineral recién descubierta, que su análisis cuantitativo siempre generaba un déficit de alrededor del siete por ciento. Tan a menudo como se repitió el análisis, el déficit permaneció aproximadamente constante y Winkler finalmente supuso que el mineral contenía un elemento hasta ahora desconocido. Después de cuatro meses de trabajo, finalmente logró 6. Febrero 1886 el aislamiento de un precipitado de sulfuro blanco, que podría reducirse en la corriente de hidrógeno a un polvo metálico. Siguiendo el planeta Neptuno previamente descubierto, Winkler inicialmente quería llamar al nuevo elemento Neptunio. Dado que este nombre ya se había utilizado para otro elemento sospechoso, lo nombró después del descubrimiento de Germanio. Winkler sugirió por primera vez que el germanio era el estibio Eka postulado por Mendeleev, mientras que Mendeleev inicialmente quería clasificarlo como cadmio Eka en lugar de silicio Eka. Después de que se determinaron otras propiedades, se confirmó que probablemente era el elemento predicho Eka-silicio. Mendeleev había derivado sus propiedades de su tabla periódica, por lo que este hallazgo contribuyó al reconocimiento de la tabla periódica:
El origen y la etimología del nombre germanio también podrían provenir de un malentendido semántico en relación con su elemento predecesor galio, porque hay dos teorías para nombrar galio. Después del primero, el químico francés Paul Émile Lecoq de Boisbaudran nombró el elemento después de la Galia, el nombre latino de su Francia natal. La segunda también es la palabra latina gallus (gallo) como la fuente del nombre, que significa le coq ("el gallo") en francés. Paul Émile Lecoq de Boisbaudran habría nombrado el nuevo elemento después de su propio nombre. Winkler supuso que el elemento anterior Gallium lleva el nombre de la nacionalidad del explorador francés. Entonces llamó al nuevo elemento químico "Germanio" en honor a su país (Latin Germania para Alemania).
Ocurrencia
El germanio está muy extendido pero ocurre solo en concentraciones muy bajas; Valor de Clarke (= contenido promedio en la corteza terrestre): 1,5 g / t. En la naturaleza, generalmente ocurre como un sulfuro (tiogermanate) y a menudo se encuentra como un compañero en los minerales de cobre y zinc (pizarra de cobre Mansfeld). Los minerales más importantes son la argyrodita. 

Extracción y producción
Según USGS, la producción anual de 2014 se estimó en 165 t, de la cual 120 t se encontraba en China. El precio de 1 kg de germanio era 2014 sobre 1.900 USD. Según la UE, el precio de 2003 era 300 USD / kg, y 2009 aumentó a 1.000 USD.
Para la representación de germanio, en particular los gases de combustión (contienen óxido de gemanio ( 

Propiedades
germanio elemental
El germanio está en la tabla periódica de la serie de semimetales, pero se clasifica por definición reciente como semiconductor. El germanio elemental es muy frágil y muy estable en el aire a temperatura ambiente. Se oxida a óxido de germanio (IV) (GeO2) solo después del recocido fuerte en una atmósfera de oxígeno. GeO2 es dimórfico y se convierte a 1033 ° C mediante la modificación del rutilo (CN = 6) en la estructura de ß-cuarzo (CN = 4). En forma de polvo, es un sólido inflamable y se puede encender fácilmente por una breve exposición a una fuente de ignición y continúa quemándose después de la extracción. El riesgo de ignición es mayor, cuanto más fina se distribuye la sustancia. En una forma compacta, no es inflamable. El germanio es bivalente y tetravalente. Los compuestos de germanio (IV) son los más estables. Del ácido clorhídrico, no se ataca la solución de hidróxido de potasio y el ácido sulfúrico diluido germanio. Sin embargo, en soluciones alcalinas de peróxido de hidrógeno, ácido sulfúrico caliente concentrado y ácido nítrico concentrado, se disuelve para formar hidrato de dióxido de germanio. Según su posición en la tabla periódica, sus propiedades químicas son entre silicio y estaño.
El germanio es una de las pocas sustancias que tiene la propiedad de anomalía de densidad. Su densidad es menor en estado sólido que en estado líquido. Su intervalo de banda es de aproximadamente 0,67 eV a temperatura ambiente.
Las obleas de germanio son considerablemente más frágiles que las obleas de silicio.
Utilizar
Electrónica
Como semiconductor, el germanio en forma de cristal único fue el material líder en el centro de electrónica de 20. Especialmente para la producción de los primeros diodos de germanio y transistores bipolares disponibles en el mercado hasta que fue desplazado por el silicio en estas áreas. Hoy en día, las aplicaciones se encuentran en la tecnología de alta frecuencia (por ejemplo, como semiconductor compuesto de germanio de silicio) y la tecnología de detección (por ejemplo, como un detector de rayos X). Las células solares de arseniuro de galio (GaAs) a veces están hechas de obleas de germanio. La constante reticular del germanio es muy similar a la del arseniuro de galio, por lo que GaAs crece epitaxialmente en cristales individuales de germanio.
Gafas y fibras
Su segunda aplicación principal es en el campo de la óptica infrarroja en forma de ventanas y sistemas de lentes hechos de germanio policristalino o monocristalino y vidrios ópticos con transmitancia infrarroja, los llamados vidrios de calcogenuro. Las aplicaciones incluyen dispositivos de visión nocturna militares y civiles, así como cámaras termográficas.
Otros usos importantes son la producción de fibras ópticas y fibras de poliéster: en las fibras de vidrio modernas para telecomunicaciones, el tetracloruro de germanio se usa en la deposición química de vapor para generar dióxido de germanio en el núcleo interno de la fibra. Esto da como resultado un índice de refracción más alto en el núcleo en comparación con el revestimiento de fibra, por lo que se garantiza la guía de las ondas de luz. En la química del poliéster, el dióxido de germanio se usa como catalizador en la producción de ciertas fibras y granulados de poliéster, especialmente para botellas de PET reciclables (PET = tereftalato de polietileno).
Medicina nuclear y tecnología nuclear
68Ge se utiliza en el generador de Gallium 68 como un nucleido padre para la producción de Gallium-68. Del mismo modo, 68Ge se utiliza como fuente para la calibración del detector en la tomografía por emisión de positrones.
Como un solo cristal de alta pureza, el germanio se usa como detector de radiación.
Germanio en suplementos nutricionales
La sustancia sesquióxido de germanio Bi (carboxietil) germanio (Ge-132) se ha promocionado como un suplemento dietético para su uso en una serie de enfermedades que incluyen cáncer, síndrome de fatiga crónica, inmunodeficiencia, SIDA, hipertensión, artritis y alergias alimentarias. Los efectos positivos en el curso de la enfermedad aún no se han demostrado científicamente.
De acuerdo con la Directiva Europea 2002 / 46 / EC sobre la aproximación de las leyes de los Estados miembros en relación con los complementos alimenticios, el germanio no debe utilizarse en complementos alimenticios. Por lo tanto, en muchos países de la UE que ya han armonizado su legislación nacional, incluidos Alemania y Austria, la adición de germanio como fuente mineral en suplementos dietéticos no está permitida.
Las autoridades competentes advierten expresamente contra el consumo de Ge-132, ya que no se pueden descartar efectos graves en la salud y muertes.
Uso medicinal de germanio.
No se ha demostrado la eficacia terapéutica de la sustancia antineoplásica spirogermanium en cáncer. No existen medicamentos aprobados con el ingrediente activo spirogermanium. En Alemania, las preparaciones farmacéuticas que contienen germanio (formulaciones), además de las diluciones homeopáticas de D4, se consideran cuestionables. Por lo tanto, su producción y entrega están prohibidas. Germanium metallicum está disponible en forma de medicamentos homeopáticos. Como parte de las preparaciones homeopáticas, se describe el lactato de citrato de germanio di-potasio.
Fisiología
El germanio y sus compuestos tienen una toxicidad relativamente baja. Se incluyen trazas de germanio en los siguientes alimentos: frijoles, jugo de tomate, ostras, atún y ajo. No es un oligoelemento esencial según el estado de la técnica. No hay una función biológica conocida para germanio. Se ha discutido una posible influencia en el metabolismo de los carbohidratos. No se conocen enfermedades por deficiencia de germanio.
toxicidad
En el pasado, el envenenamiento con germanio en humanos ocurría solo después de la ingesta de compuestos inorgánicos de germanio como suplemento dietético. Los primeros síntomas son pérdida de apetito, pérdida de peso, fatiga y debilidad muscular. Esto es seguido por un mal funcionamiento del riñón, hasta insuficiencia renal, que puede ser letal para el paciente. También se informa neuropatía periférica como consecuencia de la enfermedad.
Se informan efectos secundarios neurotóxicos transitorios cuando se toma espirogermanio en ensayos clínicos. El espiro-germanio se probó como citostático en los años 1980. Los datos de estudios en voluntarios sanos no están disponibles.
A partir de experimentos con animales, se sabe que el germanio tiene una baja toxicidad oral aguda. Los síntomas de intoxicación aguda con grandes dosis de compuestos de germanio incluyen:
- Dilatación de los vasos sanguíneos (artectasia).
- Ptosis
- cianosis
- Temblor
Finalmente, la parálisis respiratoria conduce a la muerte de los animales experimentales. Los síntomas de intoxicación crónica o subcrónica con compuestos de germanio inorgánicos son:
- la pérdida de peso
- Cambios de órganos (masa de órganos)
- Neuropatía progresiva
- daño renal
Los compuestos orgánicos de germanio mostraron una menor toxicidad, pero resultaron en la pérdida de peso de los animales experimentales y una disminución en el número de glóbulos rojos. Solo hay datos limitados sobre los efectos teratogénicos del germanio. El germanado de sodio se probó en ratas como no cancerígeno.
El mecanismo de toxicidad del germanio aún no se comprende completamente. Sin embargo, se han observado efectos patológicos específicos en las mitocondrias de las células renales y nerviosas.
interacciones
También se discute si el germanio puede mostrar interacciones con el silicio en el metabolismo óseo. Puede bloquear la acción de los diuréticos y disminuir la actividad de una serie de enzimas, como las deshidrogenasas. En experimentos con animales, los ratones muestran una mayor duración del sueño inducida por hexabarbital cuando se tratan adicionalmente con compuestos de germanio. Esto sugiere que la actividad del citocromo P450 también está restringida. Hay informes de compuestos orgánicos de germanio que bloquean la enzima de desintoxicación glutatión-S-transferasa.
Biodisponibilidad y metabolismo.
El germanio es fácilmente absorbido por el cuerpo cuando se ingiere. Se distribuye por todo el tejido corporal, especialmente en los riñones y la glándula tiroides. A diferencia de los compuestos de germanio inorgánicos, los organogermanos no se acumulan en el cuerpo humano. Sin embargo, solo hay unos pocos estudios sobre el metabolismo del germanio.
Se excreta esencialmente en la orina. La excreción a través de la bilis y las heces también tiene lugar.
Conexiones
Germanio forma Ge (II) - u. compuestos de Ge (IV) más estables, solo unos pocos tienen importancia técnica.
De los haluros de germanio también se encuentran Ge (II) - u. Representante de Ge (IV) conocido. El tetracloruro de germanio (GeCl4), un líquido con un punto de ebullición de 83 ° C, se forma al exponerse al cloruro de hidrógeno a los óxidos de germanio y es un intermedio importante en la recuperación de germanio. GeCl4 de alta pureza se utiliza en la producción de fibras ópticas de vidrio de cuarzo para producir una capa de óxido de germanio (IV) de alta pureza en el interior de las fibras de cuarzo. Para producir capas de germanio de alta pureza, también es posible utilizar la desproporción del yoduro de germanio (II) para formar yoduro de germanio y germanio (IV):
Los alemanatos son compuestos de germanio derivados de su óxido. En casi todos los minerales que contienen germanio, el germanio está presente como germanate.
Los alemanes se denominan compuestos de hidrógeno del germanio, que forman una serie homóloga de diferentes moléculas de cadena larga. El monogerman o el hidruro de germanio (GeH4) es un gas utilizado en la industria de los semiconductores para la epitaxia y el dopaje.
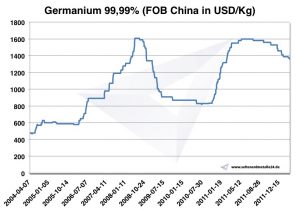
Gráfico de germanio 2004-2011

