El hafnio es un elemento químico con el símbolo Hf y el número atómico 72. Lleva el nombre del nombre latino de la ciudad de Copenhague, Hafniaen el que se descubrió el elemento. Es un metal de transición gris plateado, brillante y resistente a la corrosión que se encuentra en el cuarto subgrupo (grupo 4) o grupo de titanio en la tabla periódica.
El hafnio tiene propiedades muy similares al circonio directamente encima de él en la tabla periódica. Se desconocen las funciones biológicas, normalmente no ocurre en el organismo humano y no es tóxico.
El hafnio fue uno de los últimos elementos estables en ser descubierto en la tabla periódica. La primera indicación de la existencia de otro elemento entre lutecio y tantalio surgió de la ley de Moseley encontrada en 1912. En 1914, Henry Moseley intentó encontrar el elemento desconocido, pero esperado, con el número atómico 72 de acuerdo con esta ley en muestras de minerales de tierras raras (hoy lantánidos). Pero no tuvo éxito.
En su trabajo sobre teoría atómica publicado en 1922, Niels Bohr predijo que la serie de lantánidos con lutecio había llegado a su fin y que, por tanto, el elemento 72 debía ser similar al circonio. El hafnio pudo detectarse solo un año después: en 1923, Dirk Coster y George de Hevesy lo descubrieron en Copenhague utilizando espectroscopía de rayos X en circonio noruego. Una investigación más profunda de otros minerales mostró que el hafnio siempre está contenido en minerales que contienen circonio. Jantzen y Hevesy lograron separarlos del circonio cristalizando repetidamente los fluoruros de diamonio y dipotasio de los dos elementos. Entonces se podría obtener hafnio elemental mediante reducción con sodio.
Ocurrencia
El hafnio, con un contenido de 4,9 ppm en la corteza continental, no es un elemento muy común en la tierra. En términos de frecuencia, es comparable a los elementos bromo y cesio y más común que el oro y el mercurio, conocidos desde hace mucho tiempo. El hafnio no se encuentra de forma natural ni en sus propios minerales. Los minerales de circonio como el circonio y la baddeleyita, por otro lado, siempre contienen hafnio; la cantidad de hafnio suele ser el 2% del contenido de circonio (1-5 por ciento en peso de hafnio). Uno de los pocos minerales que contiene más hafnio que el circonio es la variedad de circón Alvit [(Hf, Th, Zr) SiO4].
De manera análoga al circonio, los depósitos de hafnio más importantes son los depósitos de circonio en Australia y Sudáfrica. Las reservas se estiman en 1,1 millones de toneladas (calculadas como óxido de hafnio).
Extracción y presentación.
Para obtener hafnio, debe separarse del circonio. Esto no es posible durante el proceso de fabricación, pero tiene lugar en un proceso separado. Para la separación se utilizan procesos de extracción. Se utiliza la diferente solubilidad de determinadas sales de circonio y hafnio en disolventes especiales. Ejemplos de esto son las diferentes solubilidades de los nitratos en tri-n-butilfosfato y la de los tiocianatos en metilisobutilcetona. Otras posibles opciones de separación son los intercambiadores de iones y la destilación fraccionada de compuestos adecuados.
Después del proceso de Kroll, el hafnio separado puede convertirse primero en cloruro de hafnio (IV) y luego reducirse a hafnio elemental con sodio o magnesio.
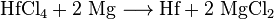
Si se requiere un hafnio aún más puro, se puede utilizar el proceso de Van Arkel de Boer. Durante el calentamiento al vacío, el hafnio reacciona inicialmente con el yodo para formar yoduro de hafnio (IV). Esto se descompone nuevamente en hafnio y yodo en un alambre caliente.

El hafnio solo se produce en pequeñas cantidades a una escala de 100 toneladas. No se produce internamente, sino que es un subproducto de la extracción de circonio sin hafnio para barras de combustible.
Propiedades
Propiedades fisicas

Estructura cristalina de α-Hf, a = 320 pm,c = 505 pm
El hafnio es un metal pesado plateado y brillante de alta densidad (13,31 g / cm3). Cristaliza en dos modificaciones diferentes según la temperatura. En condiciones normales, cristaliza en un empaquetamiento hexagonal de esferas (α-Hf) y, por lo tanto, es isotípico a α-Zr, por encima de 1775 ° C cambia a una estructura cúbica centrada en el cuerpo (β-Hf).
Si la pureza del hafnio es alta, es relativamente suave y maleable. Es fácil de trabajar rodando, forjando y martillando. Si, por otro lado, hay trazas de oxígeno, nitrógeno o carbono en el material, se vuelve quebradizo y difícil de procesar. Los puntos de fusión y ebullición del hafnio son los más altos del grupo a 2227 ° C y 4450 ° C (punto de fusión: titanio: 1667 ° C, circonio: 1857 ° C).
El metal se parece a su zirconio homólogo más ligero en casi todas las demás propiedades. Esto es causado por la contracción del lantánido, que da como resultado radios atómicos e iónicos similares (radios atómicos Zr: 159 pm, Hf: 156 pm). Una excepción es la densidad del circonio con 6,5 g / cm3 tiene un valor significativamente menor. Una diferencia técnicamente importante es que el hafnio puede absorber neutrones 600 veces mejor. Esta es la razón por la que el hafnio debe separarse para el uso de circonio en centrales nucleares.
El hafnio es superconductor por debajo de la temperatura de transición de 0,08 K.
Propiedades quimicas
El hafnio es un metal base que reacciona con el oxígeno para formar dióxido de hafnio cuando se calienta. Otros no metales, como nitrógeno, carbono, boro y silicio, también forman compuestos en estas condiciones. Se forma rápidamente una densa capa de óxido a temperatura ambiente, que pasiva el metal y lo protege de una mayor oxidación.
El hafnio es estable en la mayoría de los ácidos debido a su pasivación en condiciones normales. Se corroe rápidamente en ácido fluorhídrico; se produce una corrosión notable en ácido sulfúrico y fosfórico concentrado y caliente. Las mezclas de ácido clorhídrico y ácido nítrico, incluido el agua regia, solo deben exponerse al hafnio durante un período breve, incluso a temperatura ambiente; a 35 ° C, deben esperarse tasas de erosión de más de 3 mm / año. En bases acuosas es resistente hasta una temperatura de aproximadamente 100 ° C, la eliminación de material suele ser inferior a 0,1 mm / año.
isótopo
Hay un total de 35 isótopos y 18 isómeros nucleares de hafnio. 153Hf a 188Hf conocido. El hafnio natural es un elemento mixto que consta de un total de seis isótopos diferentes. El isótopo más común tiene una frecuencia del 35,08%. 180Hf. Sigue 178Hf con 27,28%, 177Hf con 18,61%, 179Hf con 13,62%, 176Hf con 5,27% y 174Hf al 0,16%. El único isótopo natural es 174Hf débilmente radiactivo, es un emisor alfa con una vida media de 2 x 1015 Años. Los isotopos 177Hf y 179El Hf puede detectarse con la ayuda de espectroscopía de RMN.
El isómero central 178 2mCon una vida media de 31 años, el HF es de larga duración y al mismo tiempo emite una fuerte radiación gamma de 2,45 MeV cuando decae. Ésta es la energía más alta que emite un isótopo estable durante un largo período de tiempo. Una posible aplicación es utilizar este isómero central como fuente en láseres potentes. En 1999, Carl Collins descubrió que el isómero puede liberar su energía de un solo golpe cuando se expone a los rayos X. Sin embargo, es poco probable que haya aplicaciones posibles, como explosivos.
Utilizar
Hoja de hafnio de residuos industriales
Debido a que es difícil de extraer, el hafnio solo se usa en pequeñas cantidades. El principal campo de aplicación es la tecnología nuclear, en la que el hafnio se utiliza como barra de control para regular la reacción en cadena en los reactores nucleares. El uso de hafnio tiene varias ventajas sobre otras posibles sustancias absorbentes de neutrones. El elemento es muy resistente a la corrosión y la reacción nuclear con los neutrones crea isótopos de hafnio, que también tienen secciones transversales de alta absorción. Debido al alto precio, a menudo solo es adecuado para aplicaciones militares, por ejemplo, para reactores en submarinos nucleares.
Hay algunos otros usos. El hafnio reacciona rápidamente con pequeñas cantidades de oxígeno y nitrógeno y, por lo tanto, se puede utilizar como sustancia absorbente para eliminar las cantidades más pequeñas de estas sustancias de los sistemas de vacío ultra alto. Cuando se quema, el metal emite una luz muy brillante. Por tanto, es posible utilizar hafnio en lámparas de destello con una eficiencia luminosa particularmente alta. A partir de los elementos se pueden fabricar varios compuestos muy estables y de alto punto de fusión, especialmente nitruro de hafnio y carburo de hafnio.
En aleaciones con metales como niobio, tantalio, molibdeno y tungsteno, una adición de 2% de hafnio aumenta la resistencia. Se crean materiales particularmente estables, de alto punto de fusión y resistentes al calor.
seguridad
Como muchos otros metales, el hafnio es altamente inflamable y pirofórico en su estado finamente dividido. Por otro lado, en estado compacto no es inflamable. El metal no es tóxico. Por estas razones, no es necesario observar ninguna reglamentación especial de seguridad al manipular hafnio.
Conexiones
El hafnio forma varios compuestos. En su mayoría son sales o cristales mixtos y, a menudo, tienen puntos de fusión elevados. El estado de oxidación más importante del hafnio es + IV, pero se conocen compuestos en estados de oxidación inferiores, de 0 a + III, y en complejos también se conocen estados de oxidación negativos.
El hafnio óxido (IV)
El óxido de hafnio (IV) es un sólido muy estable y de alto punto de fusión. Tiene una permitividad relativa alta de 25 (para comparación: dióxido de silicio: 3,9). Por lo tanto, se puede utilizar como dieléctrico de alta k para aislar la conexión de control (puerta) para microprocesadores. Al reducir aún más los anchos de la estructura, las corrientes de fuga se están convirtiendo en un problema cada vez mayor, porque la miniaturización de las estructuras CMOS también requiere un aislamiento de puerta más delgado. La corriente de fuga no deseada aumenta bruscamente por debajo de 2 nm debido al efecto túnel. Utilizando un dieléctrico de alta k, el espesor del dieléctrico se puede aumentar de nuevo para reducir la corriente de fuga sin que el transistor tenga una pérdida de rendimiento (reducción de la velocidad de conmutación). Por tanto, los dieléctricos más gruesos permiten una mayor miniaturización.
Otros compuestos de hafnio
El carburo de hafnio es una de las sustancias con mayor punto de fusión. Junto con el nitruro de hafnio y el boruro de hafnio, es uno de los materiales duros.
Hay algunos compuestos halógenos conocidos de hafnio. En el estado de oxidación + IV existen tanto el fluoruro como el cloruro, bromuro y yoduro. El cloruro de hafnio (IV) y el yoduro de hafnio (IV) juegan un papel en la producción de hafnio. En los estados de oxidación inferiores solo se conocen compuestos de cloro y bromo, y yoduro de hafnio (III).
El hexafluoridohafnate de potasio (IV) K2[HfF6] así como el hexafluoridohafnate de amonio (IV) (NH4)2[HfF6] puede usarse para separar el hafnio del circonio, ya que ambas sales son más solubles que los complejos de circonio correspondientes.
| General | |||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nombre, símbolo, número atómico | Hafnio, Hf, 72 | ||||||||||||||||||||||||||||||||||||||||||||||||
| serie | Los metales de transición | ||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 4, 6, d | ||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | acero gris | ||||||||||||||||||||||||||||||||||||||||||||||||
| CAS | 7440-58-6 | ||||||||||||||||||||||||||||||||||||||||||||||||
| Fracción de masa de la capa de tierra | 4,2 ppm | ||||||||||||||||||||||||||||||||||||||||||||||||
| nuclear | |||||||||||||||||||||||||||||||||||||||||||||||||
| masa atómica | 178,49 u | ||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico (calculado) | 155 (208) pm | ||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | . | ||||||||||||||||||||||||||||||||||||||||||||||||
| configuración electrónica | [Xe] 4f14 5d2 6s2 | ||||||||||||||||||||||||||||||||||||||||||||||||
| 1. ionización | 658,5 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| 2. ionización | 1440 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| 3. ionización | 2250 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| 4. ionización | 3216 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| físicamente | |||||||||||||||||||||||||||||||||||||||||||||||||
| estado físico | fest | ||||||||||||||||||||||||||||||||||||||||||||||||
| modificaciones | dos (α- / β-Hf) | ||||||||||||||||||||||||||||||||||||||||||||||||
| estructura cristalina | hexagonal | ||||||||||||||||||||||||||||||||||||||||||||||||
| densidad | 13,28 g / cm3 (25 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||
| dureza de Mohs | 5,5 | ||||||||||||||||||||||||||||||||||||||||||||||||
| magnetismo | paramagnético = 7,0 10-5) = 7,0 10-5) |
||||||||||||||||||||||||||||||||||||||||||||||||
| punto de fusión | 2506 K (2233 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||
| punto de ebullición | 4876 K (4603 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Volumen molar | 13,44 · 10-6 m3/ mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| El calor de vaporización | 630 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| calor de fusión | 25,5 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| presión de vapor | 0,00013 Pa en 1970 K | ||||||||||||||||||||||||||||||||||||||||||||||||
| velocidad del sonido | 3010 m / s en 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||
| Capacidad calorífica específica | 140 J / (kg · K) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad electrica | 3,12 · 106 A / (V · m) | ||||||||||||||||||||||||||||||||||||||||||||||||
| conductividad térmica | 23 W / (m K) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Químico | |||||||||||||||||||||||||||||||||||||||||||||||||
| estados de oxidación | 4 | ||||||||||||||||||||||||||||||||||||||||||||||||
| potencial normales | −1,505 V (HfO2 + 4 H.+ + 4 e- → Hf + 2 H2O) |
||||||||||||||||||||||||||||||||||||||||||||||||
| electronegatividad | 1,3 (escala Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||
| isótopo | |||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||
| propiedades de RMN | |||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||
| seguridad | |||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||



