El tungsteno [ˈvɔlfram] es un elemento químico con el símbolo del elemento W y el número ordinal 74. Es uno de los metales de transición, en la tabla periódica está en el sexto subgrupo (grupo 6) o grupo cromo. El tungsteno es un metal pesado blanco brillante de alta densidad, que es frágil en estado puro. De todos los metales puros, tiene el punto de fusión más alto y el segundo punto de ebullición más alto. Su uso más conocido es, por tanto, el filamento en bombillas.
Ya en el siglo XVI, el mineralogista de Freiberg Georgius Agricola describió la presencia de un mineral en los minerales de estaño sajones, lo que dificultaba considerablemente la extracción de estaño debido a la escoriación del contenido de estaño. La parte del nombre "lobo" proviene de esta propiedad, ya que el mineral "se comió" el mineral de estaño como un lobo. Si se trataba de wolframita todavía es controvertido hoy, ya que habló de la "ligereza" del mineral. Llamó al mineral lupi spumumque traducido del latín significa "espuma de lobo (s)". Más tarde se llamó Wolfram, de mhd. RAM "Hollín, suciedad", porque el mineral negro grisáceo se puede moler fácilmente y luego le recuerda al hollín. Su símbolo químico W proviene del tungsteno.
La palabra común en inglés, italiano y francés. Wolframio deriva de Tung Sten (Sueco para "piedra pesada"). Esto no significó que Wolfram mismo (sueco Volfram), pero llamado tungstato de calcio. En 1781, el químico germano-sueco Carl Wilhelm Scheele reconoció en él una sal previamente desconocida. El tungsteno puro fue producido por primera vez en 1783 por los hermanos españoles Faust y Juan José Elhuyar (que trabajaron bajo la dirección de Scheele) reduciendo el trióxido de tungsteno, que se extrae de la wolframita.
Ocurrencia
El contenido de tungsteno de la corteza terrestre es de alrededor de 0,0001 g / to 0,0064 por ciento en peso (valor de Clarke). Hasta ahora, el metal no se pudo probar en la naturaleza (en forma pura). El "Doklady Akademii Nauk" en Rusia publicó un informe sobre tungsteno sólido en 1995 sin que este haya sido examinado por la "Comisión de Nuevos Minerales, Nomenclatura y Clasificación" (CNMNC) de la IMA. Se conocen algunos minerales, especialmente óxidos y tungstatos. Los minerales de tungsteno más importantes son la wolframita (Mn, Fe) WO4 y Scheelite CaWO4. También hay otros minerales de tungsteno, como Stolzit PbWO4 y Tuneptit WO3 · H2O.
Los mayores depósitos se encuentran en China, Perú, Estados Unidos, Corea, Bolivia, Kazajstán, Rusia, Austria y Portugal. Los minerales de tungsteno también se pueden encontrar en los Montes Metálicos. Los depósitos mundiales seguros y probables son actualmente 2,9 millones de toneladas de tungsteno puro.
La ocurrencia conocida más importante de tungsteno en Europa se encuentra en Felbertal en Hohe Tauern (estado de Salzburgo en Austria).
Promoción mundial
En 2006, la producción mundial de tungsteno puro fue de 73.300 toneladas. Con mucho, el mayor productor de tungsteno es China. Más del 80% del tungsteno producido en el mundo se produce allí. Los estados con mayor producción de tungsteno (2006):
| Posición | CARGA TERRESTRE | Tasas de entrega (en toneladas por año) |
|---|---|---|
| 1 | China | 62.000 |
| 2 | Föd ruso. | 4.500 |
| 3 | Canadá | 2.500 |
| 4 | Austria | 1.350 |
| 5 | Portugal | 900 |
| 6 | Corea del Norte | 600 |
| 7 | Bolivia | 530 |
| 8 | otros paises | 900 |
Promoción en Austria
En Austria, la Scheelita de mineral de tungsteno se descubrió por primera vez en 1815/16 en el depósito de oro Schellgaden en el municipio de Muhr (estado de Salzburgo). Como resultado, se encontraron hermosos cristales de scheelita, a veces de varios centímetros de tamaño, en muchas grietas del Hohe Tauern. Ninguno de estos hallazgos fue de utilidad práctica. El gran depósito en Felbertal permaneció sin descubrir por el momento.
En 1950 se supo que aparecieron grandes cantidades de scheelita en el depósito de magnesita en Wanglalm cerca de Lanersbach / Tux (Tirol) en la parte trasera del Zillertal, que se había extraído desde 1927. Era Scheelita gruesa intercrecida con magnesita y cuarzo. En los años siguientes se extrajeron alrededor de 10.000 toneladas de mineral con un contenido promedio de óxido de tungsteno de 1,8%, lo que representó una alta calidad única en el mundo. Debido al bajo precio del mercado, la extracción de tungsteno se detuvo a fines de la década de 1960, pero se reanudó en 1971 y continuó hasta que se cerró la mina de magnesita en 1976.
1967 fue finalmente descubierto como el Scheelitvorkommen más grande de Europa en Felbertal. Las piezas de mineral presentes en las corrientes se rastrearon usando luz UV (fluorescentes Scheelite). El difícil trabajo de exploración en el terreno alpino alto (el sitio de minería más alto en Brentling en 2100 a nivel del mar) comenzó 1971, la minería inicialmente sobre el terreno se registró en Felbertal 1976 (de 1979 también minería subterránea, minería superficial 1986 set). Desde el comienzo de 1993 hasta la mitad de 1995, la minería se suspendió temporalmente debido al bajo precio de mercado del tungsteno.
El mineral de tungsteno de Felbertal se procesa en la cercana Mittersill. Desde aquí, el concentrado de scheelita llega a Sankt Martin im Sulmtal (Estiria). En el sitio de la mina subterránea de lignito Pölfing-Bergla, que se cerró en 1976, se construyó una fundición de tungsteno, en la que se ha producido óxido de tungsteno, tungsteno metálico y polvo de carburo de tungsteno a partir de concentrados de varios países desde 1977.
Los procesadores alemanes más importantes son HC Starck y el Longyear GmbH.
Extracción y presentación.
El tungsteno no se puede obtener a partir de minerales oxídicos por reducción con carbón, ya que esto da como resultado carburo de tungsteno.
La adición de solución amoniacal crea un complejo llamado paratungstato de amonio (APW). Este se filtra y luego se convierte en trióxido de tungsteno relativamente puro a 600 ° C. Óxido de tungsteno (VI) (WO3), que se reduce a tungsteno gris acero a 800 ° C bajo una atmósfera de hidrógeno:
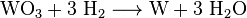
Esto produce polvo de tungsteno gris, que generalmente se compacta en moldes y se sinteriza eléctricamente en barras. A temperaturas superiores a 3400 ° C, un metal de tungsteno compacto se puede fundir en hornos eléctricos especiales con una atmósfera de hidrógeno reductor (proceso de fusión por zonas).
Propiedades
Propiedades fisicas
El tungsteno es un metal blanco brillante que se puede estirar en su estado puro y es de alta dureza, densidad y resistencia. La densidad es casi la misma que la del oro, la dureza Brinell es 250 HB, la resistencia a la tracción 550-620 N / mm2 (suave) hasta 1920 N / mm2 (difícil). El metal existe en una modificación α cúbica centrada en el cuerpo estable con un espaciado de celosía (= constante de celosía) de 316 pm a temperatura ambiente. Este tipo de estructura cristalina a menudo se denomina tipo de tungsteno. Con un como modificación β metaestable de tungsteno (distorsionado centrado en el cuerpo cúbico), por otro lado, es el óxido rico en tungsteno W3O.
Después del elemento carbono, el tungsteno tiene el segundo punto de fusión más alto de todos los elementos químicos a 3422 ° C. El punto de ebullición de 5555 ° C solo es superado por el renio de metal raro con 5596 ° C en 41 K.
El metal es un superconductor con una temperatura de transición de 15 mK.
Propiedades quimicas
El tungsteno es un metal químicamente muy resistente que apenas es atacado incluso por el ácido fluorhídrico y el agua regia (al menos a temperatura ambiente). Sin embargo, se disuelve en mezclas de ácido fluorhídrico y nítrico y mezclas fundidas de nitratos y carbonatos alcalinos.
isótopo
Se conocen 33 isótopos y 5 isómeros nucleares del tungsteno. De estos, 5 isótopos se encuentran en la naturaleza. 180W, 182W, 183W, 184W y 186W. El isótopo de tungsteno 184W tiene la mayor frecuencia. Los 5 isótopos naturales se consideraron estables durante mucho tiempo. No fue hasta 2004 que el experimento CRESST en el Laboratori nazionali del Gran Sasso logró demostrar que el isótopo era un resultado secundario de la búsqueda de materia oscura. 180W está sujeto a la desintegración alfa. La vida media es de 1,8 billones de años extremadamente larga, por lo que esta descomposición no se puede detectar en un entorno de laboratorio normal. La radiactividad de este isótopo natural es tan baja que puede ignorarse a todos los efectos prácticos. Por el contrario, los isótopos radiactivos artificiales del tungsteno tienen vidas medias cortas de entre 0,9 ms 185W y 121,2 días a las 181W.
Utilizar
Debido a su alto punto de fusión, la aplicación más importante del tungsteno se encuentra en la industria de la iluminación como filamento en lámparas incandescentes y como electrodo en lámparas de descarga de gas y en tubos de electrones.
En las lámparas incandescentes, se hace uso del hecho de que la conductividad eléctrica del tungsteno es significativamente menor que la de los metales conductores cobre y aluminio. Como resultado, el filamento delgado de tungsteno se calienta hasta que brilla, mientras que los cables más gruesos hechos de metales conductores apenas se calientan.
Tiene su segunda gran importancia como metal de aleación en la metalurgia del hierro. Forma carburos de tungsteno en aceros para herramientas, que aumentan la dureza secundaria.
Debido a su alta densidad, se utiliza para equilibrar las pesas y para proteger contra la radiación. Aunque su densidad y, por tanto, el efecto de blindaje es mucho mayor que el del plomo, se utiliza con menos frecuencia que el plomo para este propósito porque es más caro y más difícil de procesar. Además, debido a la alta densidad del tungsteno, algunos ejércitos usan municiones perforantes con un núcleo de proyectil hecho de carburo de tungsteno en lugar del uranio empobrecido más barato pero radioactivo y tóxico. Durante la Segunda Guerra Mundial, el tungsteno fue importante para la construcción de la granada del tanque alemán 40, que tenía un núcleo de tungsteno. En el futuro, la munición con núcleo de tungsteno será utilizada por el nuevo vehículo de combate de infantería Puma, que reemplazará al Marder.
Debido a su alta resistencia a la corrosión, el tungsteno también puede usarse como material para equipos en plantas químicas. Sin embargo, debido a la pobre maquinabilidad del tungsteno (el tungsteno solo puede soldarse con láser o haz de electrones), esta realización rara vez se usa. Lo mismo se aplica a una aplicación concebible en el campo de la tecnología médica.
En fisiología, especialmente en neurofisiología, los microelectrodos de tungsteno se utilizan para registros extracelulares.
Además, los electrodos para los procesos de soldadura se fabrican con tungsteno. Por ejemplo, en soldadura por resistencia, especialmente cuando se sueldan materiales como cobre, bronce o latón. También en la soldadura universal TIG (gas inerte de tungsteno), un electrodo está hecho de tungsteno o una aleación del mismo. Estos electrodos no se funden durante el proceso de soldadura. El arco se quema como plasma en un gas protector entre el electrodo y el componente. El material de relleno se suministra por separado en forma de varillas.
En el deporte, el tungsteno se usa para fabricar barriles de alta calidad para dardos, en tiro con arco se usa para hacer puntas para flechas especiales, y las cabezas de los martillos a veces están hechas de tungsteno para reducir la resistencia del aire y el radio de rotación para lanzar el martillo. Además, las placas de tungsteno se utilizan como pesos adicionales en la Fórmula 1 para lograr el peso mínimo prescrito de los coches de Fórmula 1 (incluido el aceite, los frenos y el refrigerante, así como los conductores con mono de carrera y con casco) de 620 kg (a partir de 2010). También en vela se ha utilizado en las bombas de quilla de los grandes corredores durante algún tiempo. La resistencia al agua se reduce considerablemente debido a la mayor densidad en comparación con materiales convencionales como el plomo o el hierro fundido. También hay raquetas de tenis que tienen fibras de tungsteno incorporadas en su marco de fibra de carbono. De esta manera, áreas específicas del marco de la raqueta se pueden estabilizar adicionalmente para aumentar la precisión del juego.
En la pesca con mosca, las ninfas y las serpentinas (carnada que se pesca bajo el agua) se cargan con cuentas de tungsteno que se perforan y se empujan en el vástago del anzuelo para que se sumerjan más rápido y más profundo.
Las cuerdas para instrumentos musicales a veces se enrollan con tungsteno para aumentar su peso y, por lo tanto, reducir el tono.
El tungsteno también se utiliza en el diagnóstico por rayos X como material objetivo en el ánodo. los  - y
- y  -Las líneas de la radiación característica de rayos X rondan los 59 keV y 67 keV.
-Las líneas de la radiación característica de rayos X rondan los 59 keV y 67 keV.
En la microscopía de túnel de barrido, el tungsteno se utiliza a menudo como material para la punta de la sonda.
Desde principios del siglo XXI, el carburo de tungsteno, incorrectamente denominado tungsteno, también se ha utilizado para joyería (joyería de tungsteno), p. Ej. B. anillos procesados. Esto es muy fácil de determinar a partir de la dureza y la densidad. WC tiene una dureza Mohs de 21, tungsteno solo 9,5. Hasta ahora, todas las piezas de joyería del mercado se han fabricado con carburo de tungsteno.
Fisiología
El tungsteno es utilizado como bioelemento positivo por bacterias anaeróbicas del tipo Eubacterium acidaminophilum utilizado e incorporado como cofactor en algunas enzimas. E. acidaminophilum es una bacteria fermentadora de aminoácidos que utiliza tungsteno en las enzimas formiato deshidrogenasa y aldehído deshidrogenasa. En estos organismos, el tungsteno reemplaza al molibdeno porque es mucho más común en su entorno natural (respiraderos volcánicos en el fondo del mar).
toxicología
Según el estado actual de los conocimientos, el tungsteno y sus compuestos se consideran fisiológicamente inofensivos. El cáncer de pulmón entre los trabajadores de las plantas de producción o procesamiento de metales duros se atribuye al cobalto que también está presente.
En el modelo animal se encontró que la mayor cantidad de compuestos de tungsteno ingeridos por vía oral se excreta rápidamente en la orina. Una pequeña parte del tungsteno pasa al plasma sanguíneo y de allí a los eritrocitos. Luego se deposita en los riñones y en el sistema óseo. Tres meses después de la administración, la mayoría de las pequeñas cantidades de tungsteno absorbidas por el cuerpo se encuentran en los huesos.
En 2003, en Fallon / Nevada con 16 niños que padecían leucemia desde 1997 y en Sierra Vista / Arizona con nueve niños que también padecían cáncer de sangre, se identificaron dos de los llamados grupos de cáncer, un área local con una tasa de casos de cáncer superior a la media. En ambos lugares, el agua potable tiene concentraciones excepcionalmente altas de tungsteno. Se detectaron concentraciones de tungsteno significativamente mayores en la orina del público en general. Ambos lugares son conocidos por sus depósitos de mineral de tungsteno. En las investigaciones posteriores del Centro para el Control de Enfermedades (CDC), que duraron alrededor de un año, no se pudo establecer una conexión directa entre el tungsteno y la leucemia. El tungsteno no mostró ningún efecto carcinogénico en ningún método de prueba, y no se encontraron grupos de cáncer en otros lugares de Nevada con valores de tungsteno igualmente altos en la orina de la población.
seguridad
Como polvo o polvo, es fácilmente inflamable, no inflamable en una forma compacta.
Conexiones
Óxido
El tungsteno forma varios óxidos. Entre el miembro inicial:
- Óxido de tungsteno (VI) WO3 - amarillo limón
y el miembro final:
- Óxido de tungsteno (IV) WO2 - marrón
¿Hay otros óxidos intermedios?
- W10O29 azul-violeta, rango de homogeneidad WO2,92-donde2,88
- W4O11 rojo-violeta, rango de homogeneidad WO2,76-donde2,73
- W18O49, DONDE2,72
- W20O50, DONDE2,50
Otros compuestos
- Tungstato de sodio Na2WO4
- Tungstato de circonio ZrW2O8 muestra una anomalía cuando se calienta.
- Bronces de tungsteno MxWO3; M = metal alcalino, metal alcalinotérreo, lantanoide, aproximadamente 0.3 <x <0.9 tienen conductividad eléctrica y son intensos y de diferente color según el contenido de metal.
- Tungstato de calcio CaWO4 se conoce como un mineral con el nombre de Scheelita.
- El WC de carburo de tungsteno es un compuesto similar al metal extremadamente duro. También hay carburo de diwungsteno W2C.
- Hexafluoruro de tungsteno WF6
- Plomo tungstato PbWO4
- Disulfuro de tungsteno WS2 Usar como lubricante seco (similar a MoS2)
Uso de los compuestos.
El carburo de tungsteno se utiliza como reflector de neutrones en armas nucleares para reducir la masa crítica. Los carburos de tungsteno (metal duro) se utilizan en el procesamiento de materiales debido a su alta dureza.
Los tungstatos se utilizan para impregnar las telas y hacerlas ignífugas.
Los colores de tungsteno se utilizan en la pintura, así como en la industria de la cerámica y la porcelana.
El tungstato de plomo se utiliza como centelleador moderno en física de partículas.
| General | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nombre, símbolo, número atómico | Tungsteno, W, 74 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| serie | Los metales de transición | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 6, 6, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | blanco grisáceo, brillante | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS | 7440-33-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fracción de masa de la capa de tierra | 64 ppm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| nuclear | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| masa atómica | 183,84 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico (calculado) | 135 (193) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | . | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| configuración electrónica | [Xe] 4f145d46s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. ionización | 770 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. ionización | 1700 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| físicamente | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| estado físico | fest | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| estructura cristalina | centrado en el cuerpo cúbico | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| densidad | 19,3 g / cm3 (20 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| dureza de Mohs | 7,5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| magnetismo | paramagnético = 7,8 10-5) = 7,8 10-5) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto de fusión | 3695 K (3422 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto de ebullición | 5828 K (5555 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumen molar | 9,47 · 10-6 m3/ mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| El calor de vaporización | 824 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| calor de fusión | 35,4 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| velocidad del sonido | 5174 m / s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacidad calorífica específica | 138 J / (kg · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad electrica | 18,52 · 106 A / (V · m) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| conductividad térmica | 170 W / (m K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Químico | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| estados de oxidación | 6, 5, 4, 3, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| potencial normales | −0,119 V (WO2 + 4H+ + 4e- → W + 2H2O) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| electronegatividad | 2,36 (escala Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| isótopo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| propiedades de RMN | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| seguridad | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
Frases de peligro H y P H: 228EUH: sin tarifas EUHP: 210-240-241-280-370+378 Gefahrstoffkennzeichnung
 |
| ligero inflamable |
| (F) |
Polvo Frases R y S R: 11S: 43

